1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12
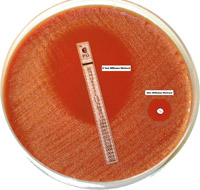
Оригинальный диско-диффузионный метод, описанный в 1966 г., хорошо стандартизован и широко используется для количественной оценки. Он рекомендован Всемирной Организацией Здравоохранения (с незначительными модификациями) в качестве референс-теста, которым следует пользоваться при рутинной работе в клинической лаборатории.
Показания к проведению исследования
Определение чувствительности следует проводить только с использованием чистой культуры микроорганизма, рассматриваемого в качестве этиологического агента инфекционного процесса. Этот микроорганизм должен быть идентифицирован (типирован). Не следует определять чувствительность контаминантов или комменсалов, относящихся к нормальной микрофлоре, или других микроорганизмов, не имеющих отношения к инфекционному процессу и, тем более, смешанных культур. Например, присутствующие в незначительных количествах в моче Escherichia coli , не рассматриваются в качестве этиологического фактора, поэтому составление антибиотикограммы не принесет пользы и даже может ввести в заблуждение. В повседневной лабораторной практике нет надобности выполнять тесты на чувствительность в тех случаях, когда возбудитель принадлежит к виду с прогнозируемой чувствительностью (см. ниже). Это относится к Streptococcus pyogenes и Neisseria meningitidis , которые до сих пор чувствительны к пенициллину (однако имеются сообщения о спорадически обнаруживаемых пенициллиноустойчивых менингококках). Если на клиническом уровне появилось подозрение на наличие устойчивости среди указанных микроорганизмов, следует направить несколько штаммов таких культур для исследования в референс-лабораторию. Если возбудитель относится к медленно растущим прихотливым микроорганизмам, например Haemophilus influenzae и Neisseria gonorrhoeae , и требует специальных сред (Основа агара для определения антибиотикочувствительности гемофильных палочек - М1259, Основа агара для гонококков - М434), применение диско-диффузионного метода без использования этих сред может дать недостоверные результаты. Появление бета-лактамазопродуцирующих вариантов у этих видов привело к внедрению специальных тестов in vitro , например, на продукцию бета-лактамаз. Мониторинг чувствительности пневмококков, гонококков и гемофильных палочек вменяется в обязанности специализированной лаборатории. Если имеет место не осложненная кишечная инфекция, вызванная сальмонеллами (кроме S. typhi или S. paratyphi), исследовать чувствительность к антибиотикам нет необходимости. Лечение антибиотиками таких инфекций не оправдано даже в тех случаях, когда применяют препараты, которые проявили активность in vitro . В настоящее время имеются убедительные свидетельства того, что антибактериальная терапия обычных сальмонеллезных гастроэнтеритов (а также большинство диарейных заболеваний не установленной этиологии) не приносит пользы больному, а лишь способствуют появлению и распространению резистентных штаммов.
Выбор препаратов для тестирования
Среди множества лекарственных препаратов, которые могли бы использоваться для лечения больного, инфицированного одним из патогенных микроорганизмов, лишь ограниченное число скрупулезно отобранных антибиотиков следует включать в перечень препаратов для определения чувствительности. Этот выбор определяется спектром антимикробной активности препарата, его фармакокинетикой, токсичностью, биодоступностью, а также стоимостью как для больного, так и для общества. В Приложении перечислены лекарственные препараты, которые могут быть использованы в различных ситуациях (см. примечания к таблицам Приложений 1-6). На практике набор антибиотиков чаще всего включает до 8 наиболее уместных в конкретной ситуации препаратов (по числу дисков, накладываемых на агар в 90- миллиметровой чашке Петри). Ниже приведены примеры таких наборов (табл. 2).
Таблица 2
Антимикробные средства для первичного и дополнительного тестирования
в зависимости от природы этиологического агента инфекции
Примечание: * гнойно-септические инфекции; ** кишечные инфекции *** неферментирующие грамотрицательные бактерии
Чувствительность в отношении препаратов, включенных в набор 2 (дополнительное тестирование), определяют только:
-по специальному запросу лечащего врача;
-если возбудитель устойчив к антибиотикам первого выбора;
-по другим причинам (включая аллергию к препарату или невозможность получения препарата), которые оправдывают постановку дополнительных тестов.
Следует периодически пересматривать списки, представленные в этой таблице, однако делать это нужно только после тщательного обсуждения вопроса с клиницистами.
На практике возникает много проблем из-за того, что клиницисты не всегда понимают, что в перечень для рутинных исследований включено лишь по одному представителю каждой группы антибактериальных препаратов. Результаты, полученные в отношении включенного в перечень препарата, затем могут быть экстраполированы на все или большинство других представителей этой группы (табл. 3)
Таблица 3
Допустимая экстраполяция результатов определения чувствительности к антимикробным средствам
|
Испытанное средство |
Испытанный микроорганизм |
Средства, на которые можно экстраполировать результат |
|
Бензилпенициллин |
Staphylococcus >spp., Neisseria gonorrhoeae> |
Феноксиметилпенициллин, фенетициллин, ампициллин, амоксициллин, бакампициллин, циклациллин, хетациллин, карбенициллин, мезлоциллин, азлоциллин, тикарциллин, пиперациллин |
|
Ампициллин |
Любой |
Амоксициллин, >бакампициллин, >циклациллин, хетациллин |
|
Ампициллин |
Enterococcus >spp.> |
Бензилпенициллин |
|
Оксициллин |
Staphylococcus >spp.> |
Все пенициллины (включая противостафилококковые), все цефалоспорины, все ингибитор-защищенные пенициллины, все карбапенемы, лоракарбеф |
|
Цефалотин |
Enterobacteriaceae> |
Цефапирин, цефрадин, цефалексин, цефаклор и цефадроксил, но не другие цефалоспорины |
|
Эритромицин |
Грамположительные кокки |
Азитромицин, >кларитромицин, >диритромицин, >рокситромицин |
|
Клиндамицин |
Любой |
Линкомицин |
|
Тетрациклин |
Любой, кроме Staphylococcus>, Enterococcus> >и Acinetobacter> >spp>.) |
Доксициклин, миноциклин хлортетрациклин, демеклоциклин, окситетрациклин, метациклин |
|
Сульфизоксазол |
Любой |
Все сульфаниламиды |
|
Цефалотин или цефазолин (>чувствительность)> |
Enterobacteriaceae> |
Чувствительность к цефалоспоринам широкого спектра |
|
Испытанное средство |
Испытанный микроорганизм |
Средства, на которые можно экстраполировать результат |
|
Бензилпенициллин |
Staphylococcus spp., Neisseria gonorrhoeae |
Феноксиметилпенициллин, фенетициллин, ампициллин, амоксициллин, бакампициллин, циклациллин, хетациллин, карбенициллин, мезлоциллин, азлоциллин, тикарциллин, пиперациллин |
|
Ампициллин |
Любой |
Амоксициллин, бакампициллин, циклациллин, хетациллин |
|
Ампициллин |
Enterococcus spp. |
Бензилпенициллин |
|
Оксициллин |
Staphylococcus spp. |
Все пенициллины (включая противостафилококковые), все цефалоспорины, все ингибитор-защищенные пенициллины, все карбапенемы, лоракарбеф |
|
Цефалотин |
Enterobacteriaceae |
Цефапирин, цефрадин, цефалексин, цефаклор и цефадроксил, но не другие цефалоспорины |
|
Эритромицин |
Грамположительные кокки |
Азитромицин, кларитромицин, диритромицин, рокситромицин |
|
Клиндамицин |
Любой |
Линкомицин |
|
Тетрациклин |
Любой, кроме Staphylococcus, Enterococcus и Acinetobacter spp.) |
Доксициклин, миноциклин хлортетрациклин, демеклоциклин, окситетрациклин, метациклин |
|
Сульфизоксазол |
Любой |
Все сульфаниламиды |
|
Цефалотин или цефазолин (чувствительность) |
Enterobacteriaceae |
Чувствительность к цефалоспоринам широкого спектра |
2. Диск с оксациллином. Оксациллин является представителем целой группы бета- лактамазорезистентных пенициллинов (включая метициллин). Часто микроорганизмы проявляют к метициллину и сходным препаратам устойчивость гетерогенного типа, т. е. большинство клеток проявляют абсолютную чувствительность и образуют широкие зоны задержки роста, в то же время резистентная часть популяции формирует мелкие колонии, растущие внутри зоны задержки роста. Устойчивые к оксациллину штаммы, как правило, устойчивы к другим бета-лактамным антибиотикам, включая многие цефалоспорины, а также карбапенемы и монобактамы.
3. Результаты, полученные при использовании диска с тетрациклином могут быть экстраполированы на хлортетрациклин, окситетрациклин и других представителей этой группы. Вместе с тем большинство тетрациклиноустойчивых стафилококков остаются чувствительными к миноциклину.
4. Ампициллин является прототипом группы пенициллинов широкого спектра действия, активных в отношении множества грамотрицательных бактерий. Поскольку они чувствительны к бета-лактамазе, их не следует использовать для определения устойчивости стафилококков. Обычно чувствительность к ампициллину проявляется и в отношении других представителей этой группы.
5. Эритромицин используется для исследования чувствительности к некоторым другим представителям группы макролидов (олеандомицин, спирамицин).
6. Аминогликозиды представляют группу химически сходных препаратов. Настоятельно рекомендуется, чтобы каждая лаборатория самостоятельно отобрала один из препаратов для первичного определения чувствительности. Другие препараты следует держать в запасе для лечения инфекционных больных с резистентной микрофлорой.
7. Нитрофурантоин используют только для лечения инфекций мочевыводящего тракта; не следует проверять чувствительность к нему микроорганизмов, выделенных из других биотопов.
Основой терапевтического действия антибактериальных препаратов является подавление жизнедеятельности возбудителя инфекционной болезни в результате угнетения более или менее специфичного для микроорганизмов метаболического процесса. Угнетение происходит в результате связывания антибиотика с мишенью, в качестве которой может выступать либо фермент, либо структурная молекула микроорганизма.
Резистентность микроорганизмов к антибиотикам может быть природной и приобретенной.
• Истинная природная устойчивость характеризуется отсутствием у микроорганизмов мишени действия антибиотика или недоступности мишени вследствие первично низкой проницаемости или ферментативной инактивации. При наличии у бактерий природной устойчивости антибиотики клинически неэффективны. Природная резистентность является постоянным видовым признаком микроорганизмов и легко прогнозируется.
• Под приобретенной устойчивостью понимают свойство отдельных штаммов бактерий сохранять жизнеспособность при тех концентрациях антибиотиков, которые подавляют основную часть микробной популяции. Возможны ситуации, когда большая часть микробной популяции проявляет приобретенную устойчивость. Появление у бактерий приобретенной резистентности не обязательно сопровождается снижением клинической эффективности антибиотика. Формирование резистентности во всех случаях обусловлено генетически: приобретением новой генетической информации или изменением уровня экспрессии собственных генов. Индуктором фенотипического проявления устойчивости может быть другой антимикробный препарат, например, под влиянием эритромицина у стафилококков может произойти экспрессия соответствующего гена и возрасти устойчивость к клиндамицину (рис. 4)
 |
Рис. 4. Слева - диск с эритромицином, справа - с клиндамицином; (Фото J.H.Jorgensen, Университет Техаса, США) |
Известны следующие биохимические механизмы устойчивости бактерий к антибиотикам:
1. Модификация мишени действия.
2. Инактивация антибиотика.
3. Активное выведение антибиотика из микробной клетки (эффлюкс).
4. Нарушение проницаемости внешних структур микробной клетки.
5. Формирование метаболического "шунта".
Среди основных клинически значимых микроорганизмов наиболее распространены следующие механизмы резистентности.
Возбудители внебольничных инфекций
• Staphylococcus spp. - устойчивость к природным и полусинтетическим пенициллинам, связанная с
продукцией бета-лактамаз.
• S. pneumoniae - устойчивость различного уровня к пенициллину (часть штаммов устойчива к
цефалоспоринам III поколения), связанная с модификацией ПСБ (пенициллин-связывающего белка);
высокая частота ассоциированной устойчивости к макролидам, тетрациклинам, ко-тримоксазолу.
• H. influenzae , M. catarrhalis - устойчивость к полусинтетическим пенициллинам, связанная с
продукцией бета-лактамаз. N. gonorrhoeae - устойчивость к пенициллинам, связанная с продукцией бета-лактамаз,
устойчивость к тетрациклинам, фторхинолонам.
• Shigella spp. - устойчивость к ампициллину, тетрациклинам, ко-тримоксазолу, хлорамфениколу.
• Salmonella spp. - устойчивость к ампициллину, ко-тримоксазолу, хлорамфениколу. Появление
устойчивости к цефалоспоринам III поколения и фторхинолонам.
• E. coli - при внебольничных инфекциях мочевыводящих путей возможна устойчивость к
ампициллину, ко-тримоксазолу, гентамицину.
Возбудители нозокомиальных инфекций
• Enterobacteriaceae - продукция БЛРС (чаще всего у Klebsiella spp.), обусловливающая клиническую
неэффективность всех цефалоспоринов; очень высокая частота ассоциированной устойчивости к гентамицину/тобрамицину;
в некоторых учреждениях тенденция к росту ассоциированной резистентности к фторхинолонам, амикацину.
• Pseudomonas spp., Acinetobacter spp., S. maltophilia - ассоциированная устойчивость к
цефалоспоринам, аминогликозидам, фторхинолонам, иногда карбапенемам.
• Enterococcus spp. - ассоциация устойчивости к пенициллинам, высокого уровня устойчивости к
аминогликозидам, фторхинолонам и гликопептидам.
• Staphylococcus spp. (метициллинорезистентные) - ассоциированная устойчивость к макролидам,
аминогликозидам, тетрациклинам, ко-тримоксазолу, фторхинолонам.